Alcaloidi
Gli alcaloidi sono una serie di composti organici contenenti azoto, biogenici (cioè di origine biologica, più spesso di origine vegetale), principalmente eterociclici. Per lo più con le proprietà di una base debole ma anche alcuni composti neutri[1] e persino alcuni debolmente acidi.[2]
Tra i costituenti delle piante più studiati e utilizzati dalla farmacologia, diversi alcaloidi sono tra le principali sostanze note che inducono effetti psicotropi quando somministrate negli organismi animali nei quali spesso causano dipendenza e tolleranza farmacologica. Si estraggono dalla pianta:
- Mediante sublimazione (evaporazione e deposito cristallino su superficie fredda);
- Mediante soluzione (cocaina in gasolio);
- Come residuo di distillazione.
Nella macerazione idroalcolica si liberano spesso se il soluto viene acidulato, per esempio con aceto, succo di limone o acido ascorbico.
Definizione[modifica | modifica wikitesto]
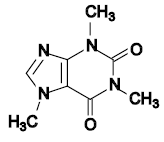

La definizione del termine alcaloide non è semplice ed è in molti casi oggetto di controversie accademiche.[3] Le difficoltà nel definire un gruppo di molecole secondarie e naturali come gli alcaloidi derivano dalla somiglianza con altri composti secondari e dal diverso ambito applicativo. Per il biologo, l'alcaloide è un prodotto naturale, puro, biologicamente attivo, un composto chimico eterociclico che contiene azoto e può avere attività farmacologica e, in molti casi, uso medicinale o ecologico.[4][5] La definizione originaria, compresa la stessa etimologia, "simile a un alcale", è stata ampliata adattandosi ai diversi ambiti di ricerca e nonostante le differenze tra i campi di ricerca in biologia, medicina e chimica si è arrivati a definizioni molto simili, dove è però necessario specificare una lunga lista di eccezioni.
Pur potendo avere caratteristiche chimiche compatibili con la definizione di alcaloide, amminoacidi, peptidi, nucleosidi, amminozuccheri e antibiotici non sono considerati alcaloidi.[1]
Una definizione soddisfacente è impossibile, dato che non esiste una divisione netta tra alcaloidi e ammine complesse naturali, ma le varie sostanze hanno in comune alcuni punti. Gli alcaloidi presentano alcune caratteristiche:
- Contengono azoto, solitamente derivato da un amminoacido.
- Sono generalmente solidi a temperatura ambiente, di sapore amaro e di colore bianco nelle composizioni purificate; un'eccezione è la nicotina che è un liquido di colore dal bianco al giallo.
- Precipitano con metalli pesanti.
- La maggior parte degli alcaloidi precipita in soluzione neutra o debolmente acida con il reagente di Mayer dando un precipitato color crema.
- Il reagente di Dragendorff con gli alcaloidi causa un precipitato arancione.
- La caffeina, un derivato della purina, non precipita come la maggioranza degli alcaloidi.
- Sono generalmente, ma non esclusivamente, basici e formano sali insolubili in acqua. La maggior parte degli alcaloidi è costituita da sostanze cristalline ben definite che si uniscono agli acidi per formare sali. Nelle piante possono esistere allo stato libero, sotto forma di sali o di N-ossidi.
- Si ritrovano in un numero limitato di piante, ad esempio la morfina esiste solo in una specie.
Solitamente derivano da vegetali, possiedono uno o più atomi di azoto (N) (generalmente in un anello eterociclico) e possiedono forti azioni fisiologiche su esseri umani e animali. Spesso sono tossici e/o psicoattivi.
Struttura[modifica | modifica wikitesto]
Ci sono tre tipi principali di alcaloidi:
- alcaloidi non eterociclici, o alcaloidi atipici (protoalcaloidi, ammine biologiche), come ad esempio la colchicina.
- pseudo-alcaloidi, derivati da terpenoidi o purine.
- alcaloidi eterociclici o alcaloidi tipici.
Gli alcaloidi sono sostanze altamente reattive con attività biologiche anche a dosaggi bassi. Alcuni tra i più importanti sono:
- gli alcaloidi a nucleo isochinolinico, tra cui si annoverano la papaverina e gli alcaloidi del curaro.

- il gruppo degli alcaloidi a nucleo fenantrenico come morfina e codeina.
- gli alcaloidi a nucleo steroideo (solasodina, tomatidina, ecc.).
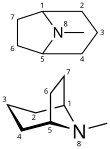
- il gruppo del tropano che comprende atropina, iosciamina e ioscina presenti nelle Solanaceae (Atropa, Datura, Hyosciamus, Mandragora). Bloccano l'attività del sistema nervoso parasimpatico.
- il gruppo dell'imidazolo.

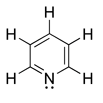
- il gruppo della piridina comprendente la piperidina, derivati dall'acido nicotinico (vitamina B3), trigonellina componente caratteristico del fieno greco e del caffè verde, lobelina presente nella Lobelia inflata, nicotina ricavabile dal tabacco, piperina nelle piante del genere Piper. Stimolano e poi bloccano tutte le attività del sistema nervoso autonomo.

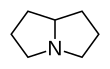
- il gruppo della pirrolizidina (alcaloide pirrolizidinico) comprendente composti molto tossici, soprattutto a livello epatico. Si trovano nelle piante delle specie Symphytum e Senecio, nella Borago, nella Tussilago farfara e molte altre.
- il gruppo dell'indolo è un gruppo complesso: comprende gli "alcaloidi animali" come adrenalina, noradrenalina e serotonina (5-idrossitriptamina - 5HT); quelli tranquillizzanti derivati dalla Passiflora; gli stimolanti uterini come l'ergotamina ed ergometrina ricavabili da funghi della specie Claviceps e il suo derivato dietilammide dell'acido lisergico (LSD); gli alcaloidi di Rauwolfia serpentaria, ipotensivi e depressivi, e molti stimolanti del sistema nervoso centrale: stricnina, yohimbina e psilocibina.

- alcaloidi a nucleo indolizidinico.

- alcaloidi a nucleo chinolizidinico.

- alcaloidi a nucleo purinico come la teofillina, la caffeina e la teobromina.

- alcaloidi a nucleo tropolonico come la colchicina.


I seguenti alcaloidi influiscono sul sistema neuromuscolare agendo sui recettori adrenergici:
- la chinolina presente nell'angostura e in piante del genere Cinchona (Rubiaceae)
- l'isochinolina derivata sempre dal genere Cinchona, molto importante
- la mescalina ricavata dalla Lophophora Williamsii (Cactaceae, chiamata comunemente Peyote)
- la papaverina e la narcotina estratte dalla specie Papaver Somniferum (Papaveraceae)
- la protopina è presente nelle piante del genere Papaver
- berberina, idrastina e canadina presenti in piante dell'ordine Ranunculales, come specie del genere Berberis (Berberidaceae), Hydrastis (Ranunculaceae) e Chelidonium (Papaveraceae)
- il gruppo della purina come caffeina, teobromina, teofillina e aminofillina presenti in piante come il Theobroma Cacao (Sterculiaceae, la pianta del cacao), Coffea Arabica (Rubiaceae, la pianta del caffè) e Camellia Sinensis (Theaceae, la pianta del tè): derivati da adenina e guanina (nome collettivo xantine). Prolungano l'emivita di molti ormoni, tra cui l'adrenalina.
- i terpenoidi presenti in piante come l'Aconitum Napellus (Ranunculaceae, altamente tossico) e la Valeriana Officinalis (Valerianaceae, tranquillante).
Alcaloidi e chemioterapia antitumorale[modifica | modifica wikitesto]
È sin dagli anni 1940 che gli alcaloidi vegetali sono oggetto di intenso studio per trovarne un'applicazione nella terapia dei tumori. Il primo a trovare impiego come tale è stata la colchicina, isolata dalla "freddolina" (Colchicum Autumnale). Questo alcaloide impedisce la polimerizzazione delle strutture cellulari chiamate "microtubuli" e ha come bersaglio proprio la proteina principale che li costituisce, la tubulina. Tuttavia è molto tossica e il suo impiego nella terapia dei tumori è oggi del tutto abbandonato.
Un'altra classe di alcaloidi è stata introdotta dopo la colchicina per la terapia dei tumori. Si tratta di alcuni alcaloidi isolati dalla Vinca rosea (o Catharanteus roseus) e risultati efficaci nella grande maggioranza dei tumori solidi umani, incluse alcune forme di leucemia/linfoma. Si tratta della vinblastina e della vincristina. Il loro meccanismo molecolare è anch'esso quello di interferire con la dinamica dei microtubuli, in modo simile alla colchicina, tuttavia sono dotate di una spiccata tossicità per le strutture nervose e in particolare per quelle periferiche. Anche per questo sono stati sintetizzati derivati meno tossici, come la vinorelbina e la vinflunina.
Uno dei loro effetti collaterali più precoci sono le nevriti e le neuropatie che comprendono parestesie, pallestesie, dolori di tipo folgorante e difetti trofici. La ragione di questi effetti risiede nella loro stessa base d'azione: interferendo con i microtubuli delle strutture nervose impediscono il trasporto di proteine essenziali e di alcuni nutrienti a livello periferico e da questo deriva la sofferenza nervosa. Un metodo efficace per tamponare questo effetto è la buona idratazione del paziente e la supplementazione con vitamine del gruppo B, tutte con azione benefica sul trofismo dei nervi periferici.
Un'altra classe di alcalodi impiegata correntemente nella chemioterapia è quella dei "taxani", alcaloidi isolati dal Taxus canadensis e risultati molto attivi in diversi carcinomi e sarcomi umani, mentre il loro impiego nelle emopatie maligne è nullo. Il loro meccanismo d'azione è esattamente opposto a quello della colchicina: invece di impedire la costruzione dei microtubuli, impediscono il loro disassemblamento per ricreare nuove strutture microtubulari (effetto di "congelamento" strutturale). Il primo a essere sperimentato fu il paclitaxel e poi sono stati sintetizzati derivati con minore tossicità e maggiore biodisponibilità, come il docetaxel.
Un ultimo gruppo che è entrato recentemente nella fase di sperimentazione clinica sono gli alcalodi isolati dalla Camptotheca acuminata. Il prototipo è la camptotecina, che ha come bersaglio non direttamente il DNA, ma un enzima nucleare deputato alla stabilizzazione dell'intero genoma, la topoisomerasi. È risultata attiva contro molte forme di tumore solido e sono stati sintetizzati anche dei suoi derivati leggermente più efficaci e contemporaneamente meno tossici. Tre di questi sono la 9-nitro-camptotecina, il TPT o Topotecano, il CPT-11 o Irinotecano e l'Edotecarin.
Negli anni 1980 sono stati studiati più di una trentina di alcaloidi provenienti da varie fonti vegetali. Alcuni di essi sono risultati estremamente efficaci nell'eliminazione di tumori e leucemie indotte in modelli animali, tuttavia la loro tossicità sistemica è risultata ancora troppo elevata per permetterne l'introduzione nella terapia umana. Tra essi i più efficaci sono risultati:
- le acronicine (dall'Acronychia baueri)
- la talicarpina (dal Thalictrum dasycarpum)
- la tetrandrina (dalla Stephania tetrandra)
- la cefarantina (dalla Stephania cepharanta)
- la ruteacarpina (dalla Evodia ruteacarpa)
- la ellipticina (dalla Derria elliptica)
Quest'ultima molecola ha suscitato negli ultimi cinque anni un intenso interesse nel campo dell'oncologia. Infatti il suo 9-idrossiderivato può legare alcune forme mutate (inattive) del famoso oncosoppressore p53, responsabile della comparsa di tumori solidi, e ripristinarne la funzione corretta. Sono in corso studi di laboratorio per capire il meccanismo con cui questa molecola possa interferire con la progressione tumorale attraverso la manipolazione della proteina p53. Anche per quanto riguarda le acronicine, il loro derivato S 23906 è attualmente in fase II di sperimentazione (trial clinici) perché risultato molto promettente.
Note[modifica | modifica wikitesto]
- ^ a b IUPAC - alkaloids (A00220), su goldbook.iupac.org. URL consultato il 26 febbraio 2020.
- ^ B. Franck, The Alkaloids, Chemistry and Physiology. Von R. H. F. Manske. Bd. VIII: The Indole Alkaloids. Academic Press Inc., New York-London 1965. 1. Aufl., 861 S., geb. $ 32,000, in Angewandte Chemie, vol. 79, n. 3, 7 febbraio 1967, pp. 159-159, DOI:10.1002/ange.19670790329. URL consultato il 26 febbraio 2020.
- ^ Aniszewski, Tadeusz., Definition, in Alkaloids - secrets of life : alkaloid chemistry, biological significance, applications and ecological role, Elsevier, 2007, p. 1, ISBN 978-0-444-52736-3, OCLC 162587596. URL consultato il 26 febbraio 2020.
- ^ R. HEGNAUER, Chemical Plant Taxonomy, Elsevier, 1963, pp. 389-427, ISBN 978-0-12-395540-1. URL consultato il 26 febbraio 2020.
- ^ E. Lovell Becker e I. Landau, International Dictionary of Medicine and Biology, in Journal of Clinical Engineering, vol. 11, n. 2, 1986-03, p. 134, DOI:10.1097/00004669-198603000-00007. URL consultato il 26 febbraio 2020.
Bibliografia[modifica | modifica wikitesto]
- T. W. Graham Solomons, Chimica organica, 2ª ed., Bologna, Zanichelli, 2001, pp. 892-900, ISBN 88-08-09414-6.
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikizionario contiene il lemma di dizionario «alcaloide»
Wikizionario contiene il lemma di dizionario «alcaloide» Wikimedia Commons contiene immagini o altri file su alcaloide
Wikimedia Commons contiene immagini o altri file su alcaloide
Collegamenti esterni[modifica | modifica wikitesto]
- alcaloidi, su Treccani.it – Enciclopedie on line, Istituto dell'Enciclopedia Italiana.
- alcalòide, su sapere.it, De Agostini.
- (EN) alkaloid, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- (EN) IUPAC Gold Book, "alkaloids", su goldbook.iupac.org.
- Alcaloidi, in Treccani.it – Enciclopedie on line, Roma, Istituto dell'Enciclopedia Italiana.
| Controllo di autorità | Thesaurus BNCF 9880 · LCCN (EN) sh85003598 · GND (DE) 4068543-3 · BNF (FR) cb11944043x (data) · J9U (EN, HE) 987007293926805171 · NDL (EN, JA) 00560348 |
|---|